文章图片
▲ IgG类抗体的结构示意图
已有众多研究证明 , Fc的三个氨基酸(M252Y/S254T/T256E [YTE])突变 , 会大幅延长抗体的半衰期[9] 。 因此 ,腾盛华创的研究人员给P2C-1F11/P2B-1G5的Fc段做了YTE改造 , 安巴韦单抗/罗米司韦单抗就正式诞生了 。
改造后 ,安巴韦单抗/罗米司韦单抗的半衰期是普通抗体的2-3倍 , 即从21天延长到46-76天[10] 。 这种“超长待机”的能力 , 为安巴韦单抗/罗米司韦单抗以后用于预防新冠感染的临床研究打下了坚实的基础 。
值得一提的是 , 从筛选中和抗体 , 到安巴韦单抗/罗米司韦单抗完成升级 , 仅用了短短半年时间 。 2020年7月 , 安巴韦单抗/罗米司韦单抗正式获得中国临床批件 , 完成首次人体给药 。
住院/死亡风险降低80% , 疗效居世界前列
那么安巴韦单抗/罗米司韦单抗的疗效究竟如何?与国外已获批的中和抗体疗法相比 , 又有哪些独到之处呢?
要解答上面这两个问题 , 我们得从今年1月份 , 由美国国立卫生研究院(NIH)下属国家过敏症和传染病研究所(NIAID)主导的ACTIV-2研究说起 。
ACTIV-2是一项全球多中心、随机、双盲2/3期临床研究[11] , 评估安巴韦单抗/罗米司韦单抗联合疗法对有症状、非住院、且有发展为重症风险因素的成年新冠患者的安全性和有效性 。
这个研究于2021年的1到7月之间(Delta和Lambda流行期) , 在全球范围内招募了847例患者 , 所有受试者按照1:1随机分组 , 最终837例患者分到抗体治疗组或安慰剂组 。
8月25日 , 腾盛博药发布中期分析数据显示 , 与安慰剂组相比 , 安巴韦单抗/罗米司韦单抗治疗组患者的住院及死亡风险降低78%(P值<0.00001);12月5日发布的 三期最终分析数据显示 , 安巴韦单抗/罗米司韦单抗治疗组患者的住院及死亡风险降低80%(P值<0.00001) ,治疗组受试者在28天的治疗期内无死亡病例 , 而安慰剂组有9例死亡[12] 。
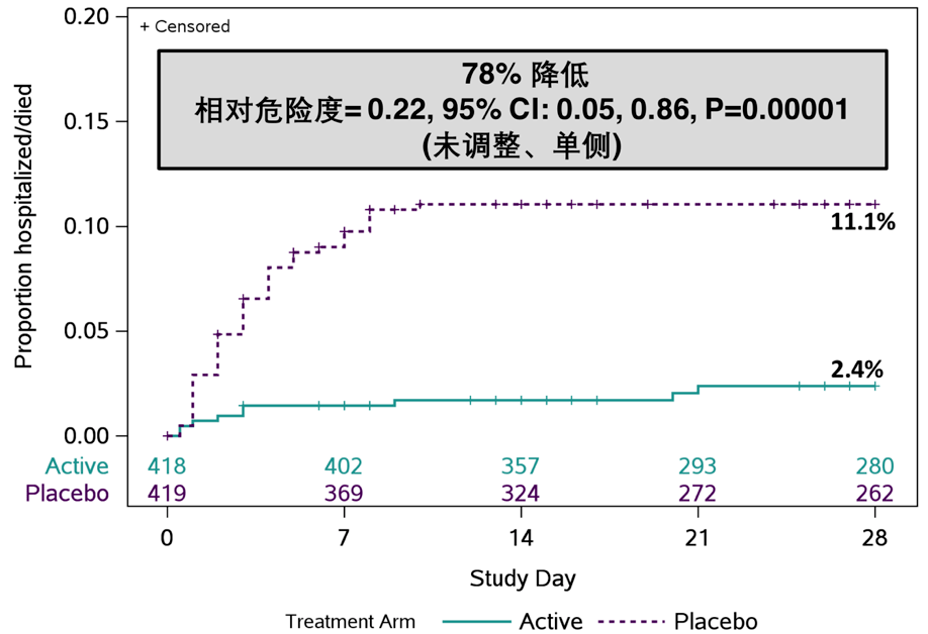
文章图片
▲ 第28天时住院/死亡的累计发生率(图示为8月25公布的研究中期分析数据)
从有效性数据上看 , 与已经获得FDA紧急使用授权的Etesevimab/Bamlanivimab [13]、Casirivimab/Imdevimab[14]和Sotrovimab[15,16]相比 ,安巴韦单抗/罗米司韦单抗毫不逊色 , 达到了世界一流水平 。
而且值得一提的是 ,与上述药物的临床研究相比 , ACTIV-2研究对照组患者的住院/死亡累计发生率更高 , 提示入组患者病情更重 。 此外 ,接受安巴韦单抗/罗米司韦单抗治疗的患者从发病到入组的时间为≤10天 , 相对其他研究更长[13-16] 。
不难看出 , 在取得同等水平疗效数据的情况下 , 安巴韦单抗/罗米司韦单抗治疗的患者病情更严重 , 而药物治疗有效的应用时间窗更长 , 更加符合实际临床操作 , 因此 这一组合有可能在抗疫中发挥更大的作用 。
从治疗到预防 , 潜力无限
从前面的内容不难看出 , 中和抗体在新冠肺炎的治疗中发挥着重要的作用 。 实际上 , 中和抗体的作用远不止这些 , 在预防感染新冠的战场上 , 例如暴露后预防和暴露前预防 , 中和抗体也能发挥重要的作用 。
顾名思义 , 暴露后预防就是曾与新冠感染者有过接触 , 也就是我们比较熟悉的密接者和次密接者 。 这些人即使接种过疫苗 , 也存在突破性感染的风险 。
今年1月份 , 礼来发布了重组中和单抗Bamlanivimab暴露后预防的研究数据 。 研究结果显示 , 与安慰剂相比 ,使用Bamlanivimab的受试者出现有症状新冠感染的风险降低了57%[17] 。
- 疫苗|【992 | 速看】传播能力有所增强!有关奥密克戎变异株,最新解答来了!
- 相关|【中国实用外科杂志】肥胖代谢病合并甲状腺癌外科治疗中国专家共识(2021版)
- 中国雄安官网1月14日电(李元闯)在雄安新区安新县|家乡雄安丨杨宏记:村民致富路上的“带头人”
- 春节是中国人心中最重要的传统节日之一|椒盐皮皮虾的做法,外酥里嫩,咸香入味,寓意着大富大贵
- 张奶奶|为危重患者保驾护航!全院大会诊助力我院综合诊疗能力不断提升
- 幽门|阿里健康上线国内首个幽门螺杆菌自测产品“幽幽管”
- 双下肢|中国家长最喜欢的兴趣班,却没人提醒你它有多危险!
- 考试|“双减”后首个期末考试不该再现“聪明药”
- 生活质量|中国援建考斯玛中柬友谊医院将启用
- 来源:西安日报...|叮!中国疾控的寒假健康提示来了,家长请查收
