心血管代谢性疾病已成为导致人类死亡的头号杀手 。 为了解决心血管代谢性疾病的发病机制和临床治疗问题 , 武汉大学教授李红良团队近十多年来综合运用生物大数据、疾病动物模型、人工智能药物设计等前沿技术 , 发现花生四烯酸通路是心脏、肝脏缺血再灌注损伤和脂肪肝炎的核心发病机制 , 并进一步找到了最关键的治疗靶点—12-脂氧合酶(ALOX12) 。 根据这一重要靶点 , 研究团队开发出了3种高效安全的先导化合物 , 其中一种全新的小分子化合物(IMA-1)可精准靶向ALOX12-ACC1蛋白相互作用 , 显著抑制小鼠和食蟹猴脂肪肝炎发生发展 。 更为重要的是 , 这一新开发的先导化合物不会引起高血脂等副作用 。 系列研究突破性解决了靶向ACC的副作用问题 , 破解了靶向ACC治疗脂肪肝炎的困境 。
系列成果于2021年12月15日作为封面文章在《科学·转化医学》杂志背靠背同时发表 , 并被列为亮点研究写入12月17日出版的《科学》杂志特刊 。 同时 , 科研团队还首次发现ALOX12小分子抑制剂ML355可有效改善小鼠、巴马猪和恒河猴的心脏缺血再灌注损伤 , 显著提升心功能 , 为深入探索心脏缺血再灌注损伤、改善心梗患者预后、提高患者生存率提供了重要支撑 。
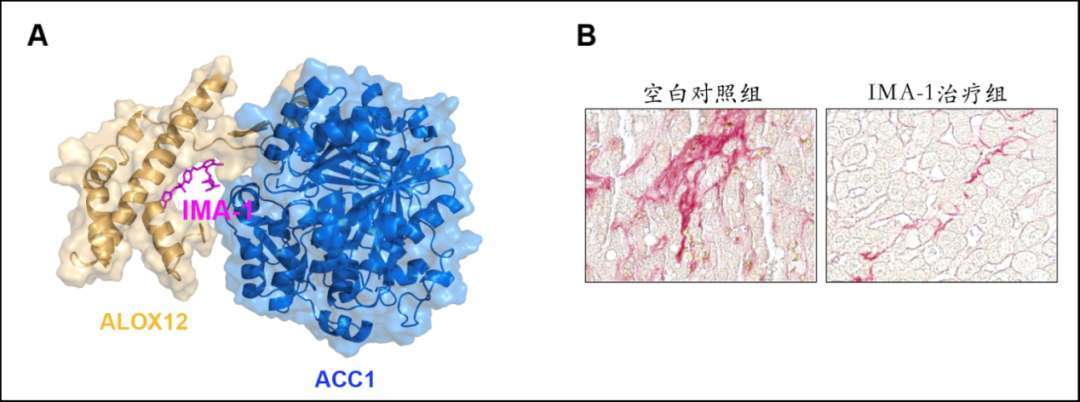
文章图片
图1: A. IMA-1抑制ALOX12和ACC1蛋白互作结构图;图B. IMA-1治疗脂肪肝炎效果(红色染色区域代表肝脏纤维化程度)
肥胖、2型糖尿病以及NAFLD是代谢综合征的主要诱因 , 为了更好地解决这些健康威胁 , 李红良教授团队对疾病发病机制进行了深入探索 。 采用大规模系统生物学筛选分析、免疫荧光、过表达腺病毒处理等先进技术 , 研究团队发现TMBIM1是通过降低PPARγ的稳定性而抑制脂肪生成 , 是一种有效抑制脂肪生成的全新因子 , 为加深脂肪生成调控机制的认识提供了潜在分子靶点与新思路;发现Nemo样激酶(NLK)作为一种新型肝糖异生负调控因子 , 促进CRTC2和FOXO1核输出 , 在糖异生调节网络中起着关键作用 , NLK可能成为2型糖尿病的潜在治疗靶点;为了进一步阐明NAFLD的发病机制 , 团队还发现了一系列重要分子 , 如MAVS、SNX8、RNF5、RGS5等 , 它们都是NAFLD发展的关键分子 , 是NAFLD预防和治疗的潜在药物靶点 。 系列研究成果发表在Cell Metabolism、Hepatology等国际权威杂志 。
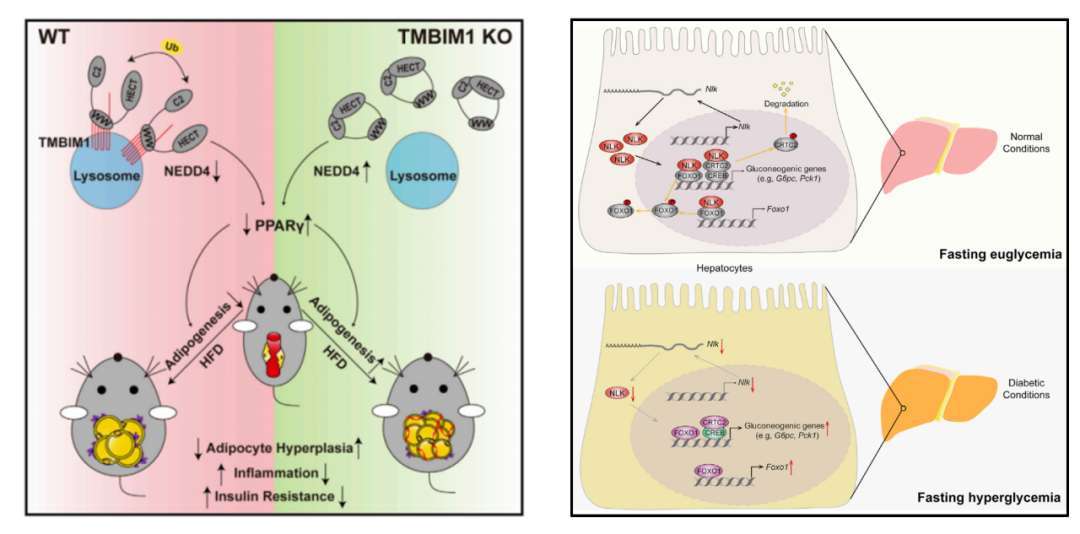
文章图片
图2:TMBIM1调控脂肪生成新机制 图3:NLK促进CRTC2和FOXO1核输出
心血管疾病已成为全球死亡率增加的主要原因 。 近年来 , 随着社会的发展、人民生活水平的提高以及生活方式的改变 , 代谢危险因素已成为心血管疾病发病率逐年上升的重要原因 。 李红良教授团队通过应用全球疾病负担研究的方法框架 , 分析了1990年至2019年全球缺血性心脏病疾病负担和15个相关的一般危险因素 , 发现代谢危险因素已成为缺血性心脏病的主要驱动因素 , 并为不同国家及地区缺血性心脏病防治政策的制定提供了有力依据 。 此外 , 团队还发表了相关综述总结了代谢因素驱动多种心血管疾病发展的流行病学趋势和病理生理机制等 。 系列研究成果发表在Cell Metabolism、Cir Res等国际权威杂志 。
据了解 , 模式动物研究所是支撑武汉大学医学领域的学科发展、科研水平提升和高层次人才培养的重要载体 , 同时也是提供医学研究引领性服务的高端科研机构 。 过去十三年来 , 团队服务人民医院心内科、肿瘤科、消化内科等科室人员1000余人 , 各科室累计利用研究所平台发表论文700余篇 , 申请获得并开展国家项目100多项 。 据2021年10月发布的“2020年度中国医院/中国医学院校科技量值(STEM)”排行榜 , 人民医院心血管学科排名提升至历史最高第3位;心血管学科科技产出全国第2位 。 据国际机构检索及分析 , 全球心血管领域2020年研究活跃度 , 人民医院居全球第4 , 中国第3 。
- 治疗|血肌酐高,我们的身体会有什么不适?看看他们是怎么理解的
- 检测|西安海棠职业学院人物风采:致敬我们身边的抗疫先锋
- 烟熏肉|美国哈佛大学最新研究:我国结直肠癌多是吃出来的,远离3种食物
- 朱南孙|99岁国医透露:这2种食物我从不吃!值得记住的私家调理方!
- 清凉油85%效用,你还不知道!原来我们一直在暴殄天物
- 杂蔬|晒晒我家三口人晚餐,不到30元做了3道菜,可比吃外卖强多了
- 喝水|世界上最有效的“长寿药”,还是免费的,我们每天都喝却经常犯错
- 今天我要给大家分享一个|晒干的腊肉,别傻傻的放冰箱,教你一招,放一月不变质还更香
- 代谢|糖尿病是“懒出来”的?医生:教你3个不费力的小妙招,血糖乖乖降
- 老渔民教我一招,不加一滴水,煮出的白灼虾比饭店好吃
