【肿瘤|《自然》:“加热”恶性胸腔积液,辅助免疫治疗!】恶性胸腔积液(MPE)是晚期肿瘤的常见表现之一 , 以非小细胞肺癌(NSCLC , 36%)、乳腺癌(26%)和淋巴瘤(13%)最为常见[1] 。 MPE会引起患者咳嗽、胸痛、呼吸困难和乏力等症状 , 严重影响患者的生活质量和预后 , 有研究表明 ,MPE患者的中位生存期仅为5个月[2] 。
MPE的传统治疗方法主要以缓解呼吸困难症状为主 , 如胸腔穿刺引流、胸膜固定 , 但疗效欠佳 , 且不良反应多、复发率较高 。
随着免疫时代的到来 , 专家们根据免疫微环境中CD3和CD8淋巴细胞的浸润程度 , 将肿瘤分为“热”肿瘤(高度浸润)和“冷”肿瘤(非浸润性) , “热”肿瘤对免疫治疗的反应性更好 , 将“冷”肿瘤变热成为肿瘤免疫治疗的新突破口[3] 。MPE的肿瘤微环境中含有大量促瘤髓系免疫细胞和免疫抑制细胞因子 , 具有较强的免疫抑制作用 , 属于“冷”肿瘤[1] 。
MPE的免疫治疗除了PD-1/PD-L1抑制剂[4] , 科学家还尝试通过胸腔内注射免疫刺激物 (如细菌抗原、促炎细胞因子、溶瘤病毒或腺病毒细胞因子基因)来增强MPE的抗肿瘤免疫[5, 6] 。 但这些方法要么不能很好地增强免疫 , 要么引起严重的不良反应 。 因此 ,寻求一种能有效地将“冷”肿瘤变热的新胸腔内治疗方法 , 对于改善MPE的免疫治疗至关重要 。
为此 , 来自 美国维克森林医学院的Dawen Zhao教授团队开发了一种新的胸腔内治疗方法 , 这项研究成果近期发表在 Nature Nanotechnology 杂志上[7] 。
他们合成了一种 含环二核苷酸(CDN)的脂质体纳米颗粒(LNP-CDN) , 胸腔内注射LNP-CDN能够改善肿瘤的“冷”免疫 , 提高肿瘤免疫治疗的疗效 。

文章图片
▲ 论文首页截图
我们都知道 , 干扰素基因刺激因子(STING)通路在抗肿瘤免疫中起着重要作用 , 而CDN能够连接STING , 并激活STING途径和I型干扰素(IFN)的产生 , 发挥抗肿瘤免疫作用 。 基于此 ,有研究发现肿瘤内注射CDN可以增强实体肿瘤的抗肿瘤免疫效果 , 但还没有研究探索胸腔内注射CDN的作用 。
科学家们注意到在MPE中使用CDN存在的一个问题: 游离CDN不稳定 , 易被外核苷酸焦磷酸酶/磷酸二酯酶(ENPP1)降解 , 不巧的是 ,MPE中的ENPP1水平很高 。 这使得胸腔内注射游离CDN受到了限制 。
为了解决这一问题 , Zhao教授团队合成了一种 LNP-CDN , 这种纳米颗粒能保护CDN不被MPE的酶降解 , 使其在MPE中表现出良好的药代动力学特征 , 并可以 选择性靶向胸腔内的巨噬细胞和树突状细胞 。
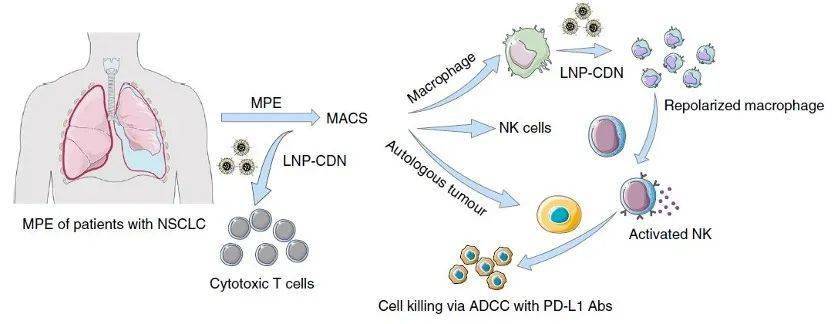
文章图片
Zhao教授团队通过建立Lewis肺癌小鼠的MPE模型 , 向小鼠的胸腔内注射被DiR标记的LNP-CDN后 , 发现 LNP-CDN主要停留在胸部 , 持续至少48小时 , 血液和其他主要器官也有少量的LNP-CDN 。 然后收集MPE中的免疫细胞 , 他们发现 LNP-CDN能够靶向MPE中的CD11c+巨噬细胞和树突状细胞 。 不仅如此 ,LNP-CDN还可以增强肿瘤引流淋巴结中的细胞毒性T细胞交叉活化 。
为了了解胸腔内注射LNP-CDN对MPE中免疫细胞和免疫反应的影响 , Zhao教授团队进行了单细胞RNA测序、流式细胞术和ELISA 。 他们发现注射48小时后 , MPE中出现20个不同的细胞簇 , 包括肿瘤细胞、巨噬细胞、中性粒细胞、树突状细胞、NK细胞、CD4+T细胞、CD8+T细胞和B细胞等各种免疫细胞 。
其中巨噬细胞最多 , 可分为6个亚群 ,LNP-CDN可以诱导巨噬细胞复极化和分型 , 使M2向M1转化 。 此外 , 他们还发现 LNP-CDN和PD-L1抑制剂联合胸腔内注射可以进一步增加M2向M1的转化 。
- 卫生室|《乡村医生诊疗口袋书(先行本)》面世
- 脏腑|重庆肿瘤专科医院:中医帮你调和气血,平衡阴阳
- 预防肿瘤|夜里温度下降孩子睡不好,多吃营养菜,补虚暖胃,提高抵抗力
- 致癌|十多种肿瘤与“吃”密切相关,看完请注意避开!
- 解读|《浙江省医院门诊管理办法》政策解读
- 肿瘤|健康大讲堂丨肿瘤专家袁芃:乳腺癌病因尚不明确 防治重在“三早”
- 廉东波|《健谈》观点丨浅表性胃炎三五年复查一次 萎缩性胃炎一年一查
- 香港|广州复大肿瘤医院案例966:香港胰腺癌患者赴广州就医重获新生
- 家长|杭州《青少年皮肤健康状况调研》发布,近半青少年受皮肤疾病困扰
- 胶质瘤是脑内最常见的恶性肿瘤之一|胶质瘤能治好吗?复发后有必要再次手术吗?医生说了实话
