首批用于自测的新冠抗原检测产品获批!
3月12日 , 国家药监局发布通告 , 批准南京诺唯赞、北京金沃夫、深圳华大因源、广州万孚生物、北京华科泰生物的新冠抗原产品自测应用申请变更 。 自此五款新冠抗原自测产品正式上市 。
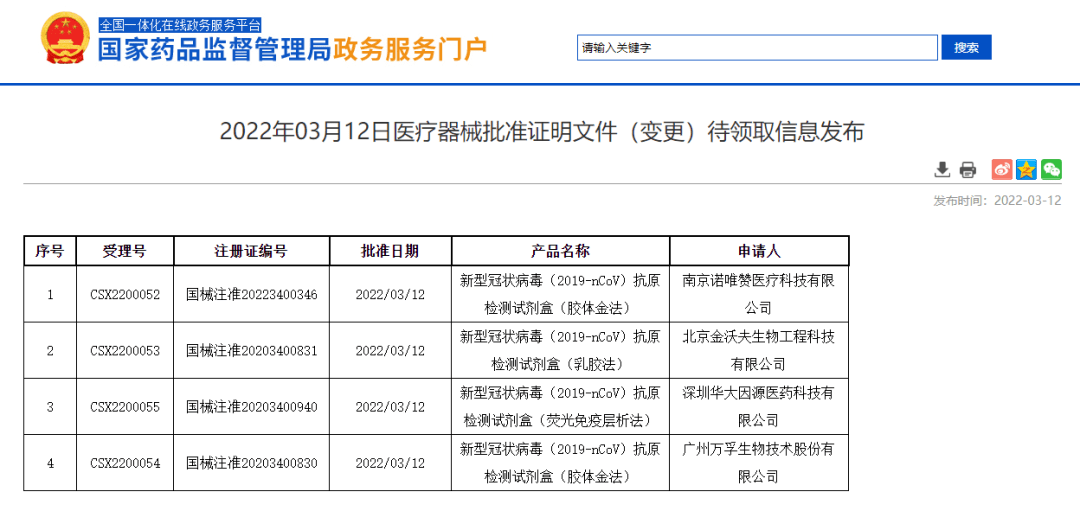
当天 , 国家药监局政务门户网站发布的最新的待领取信息显示 , 4款新冠抗原检测试剂盒产品获得的医疗器械批准证明文件(变更)待领取 , 批准时间均在3月12日 , 涉及4家公司 , 包括南京诺唯赞生物科技股份有限公司(诺唯赞 , 688105)全资子公司南京诺唯赞医疗科技有限公司、广州万孚生物技术股份有限公司(万孚生物 , 300482)、华大基因(300676)子公司深圳华大因源医药科技有限公司、北京金沃夫生物工程科技有限公司 。
文章图片
加上此前一天获准变更的北京华科泰 , 获准变更的厂商已经增至5家 。

文章图片
3月11日 , 国家药监局政务门户网站发布的待领取信息显示 , 北京华科泰生物技术股份有限公司的新冠抗原检测产品的医疗器械批准证明文件(变更)待领取 , 批准日期为3月11日 。
目前 , 国内共有5家企业的5款新冠抗原检测产品获批 , 正是上述5款变更信息的产品 。 此前 , 这些产品仅获批用于专业人员使用 , 而非自测 。 此次公布的变更待领取信息 , 国家药监局并未披露产品变更的详细内容 , 有业内观点认为 , 此次变更的信息可能是允许用于居民自测 。
3月11日 , 国家卫生健康委员会发布《新冠病毒抗原检测应用方案(试行)》 , 明确在核酸检测基础上 , 增加抗原检测作为补充 , 其中提到社区居民有自我检测需求的 , 可通过零售药店、网络销售平台等渠道 , 自行购买抗原检测试剂进行自测 。 (详情)
短短一天之后 , 五款新冠抗原自测产品正式上市 。
试行方案对基层医疗卫生机构抗原检测应用、隔离观察人员抗原检测应用、社区居民抗原检测应用进行了详细介绍 。 根据方案 , 在基层医疗卫生机构使用抗原检测有专业人员进行样本采集 , 而隔离观察人员和社区居民应用则涉及到自测问题 。
这是首次明确社区居民自测新冠的相关政策 。
01
自测结果能取代核酸吗?
不能 。
此次通知明确 , 经研究 , 国务院应对新型冠状病毒肺炎疫情联防联控机制综合组决定在核酸检测基础上 , 增加抗原检测作为补充 。 核酸检测依然是新冠病毒感染的确诊依据 。
试行方案中的《新冠病毒抗原自测基本要求及流程》也强调 , 抗原检测一般用于急性感染期 , 即疑似人群出现症状 7 天之内的样本检测 。 疑似人群抗原阳性及阴性结果均应当进行进一步的核酸检测 , 阳性结果可用于对疑似人群的早期分流和快速管理 , 但不能作为新冠病毒感染的确诊依据 。
02
哪些人可以自测?
三类人群:
①到基层医疗卫生机构就诊 , 伴有呼吸道、发热等症状且出现症状5天以内的人员;
②隔离观察人员 , 包括居家隔离观察、密接和次密接、入境隔离观察、封控区和管控区内的人员;
③有抗原自我检测需求的社区居民 。
03
新冠自测频率如何确定?
视人群来定 。
对于隔离观察人员 , 在隔离观察期按照现行的有关防控方案要求开展核酸检测 , 并在前5天每天进行一次抗原自测 。
对于社区居民 , 有自我检测需求的可以自行购买进行自测 。 抗原检测阴性的 , 无症状的居民可密切观察 , 需要时再进行抗原检测或核酸检测;有症状的居民 , 建议尽快前往设置发热门诊的医疗机构就诊 , 进行核酸检测;如不便就诊 , 则应当居家自我隔离 , 避免外出活动 , 连续5天每天进行一次抗原自测 。
- 夏季很多豆类蔬菜都大量上市了|豆角饺子的做法,掌握这2个重点,就能做出皮薄馅多超好吃的饺子
- 抗原|自测试剂盒正式上市!还需要去做核酸检测吗?
- 诺唯|重磅!百亿零售药店将开卖新冠自测产品,15分钟出结果!更有A股公司今日“首发”?多家零售药企紧急备货!
- 广州|15分钟可出结果!5款新冠抗原自测产品获批上市,2款广东造
- 记忆力|大量上市!天然“补脑豆”防痴呆、护血管,一年只有现在有!错过太可惜!
- 生物|新冠抗原自测产品,正式上市!
- 检测|刚刚宣布!正式上市!
- 产品|【生活】5款新冠抗原自测产品上市 | 淘宝内测修改账号名
- 方案|官宣!正式上市
- 新冠|新冠抗原自测产品,正式上市!
